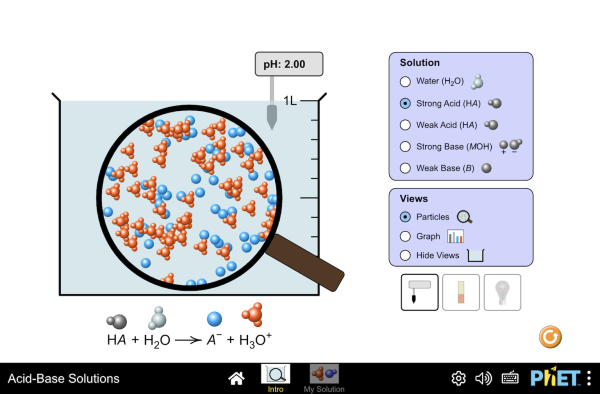
Versuch Ionenverbindungen und Salze 2016 06 16 Leitfähigkeit von dest Wasser vor und nach Zugabe
Unterrichtsmitschrift von Sarah Schiemann am 5.12.und 6.12.2016


https://phet.colorado.edu/sims/html/acid-base-solutions/latest/acid-base-solutions_de.htm
Im Oktober 2018 verfügbar unter: https://phet.colorado.edu/de/simulation/acid-base-solutions
Vgl. auch: https://phet.colorado.edu/

Exkurs: Massenwirkungsgesetz
Das Massenwirkungsgesetz (Abkürzung „MWG“) besagt, dass bei einer chemischen Reaktion im chemischen Gleichgewicht der Quotient aus
- dem Produkt der Konzentrationen der Reaktionsprodukte und
- dem Produkt der Konzentrationen) der Ausgangsstoffe
einen für die betrachtete Reaktion konstanten und charakteristischen Wert hat.[1]
Das MWG gilt für Reaktionen, die reversibel sind. Die resultierende Gleichgewichtskonstante, auch Massenwirkungskonstante genannt, hat unter gegebenen Bedingungen einen für die betrachtete Reaktion spezifischen Wert, der nur über die äußeren Bedingungen (z. B. Temperatur oder Druck) beeinflusst werden kann.
Das Massenwirkungsgesetz für die Reaktion
wird wie folgt formuliert:
Quelle: Seite „Massenwirkungsgesetz“. In: Wikipedia, Die freie Enzyklopädie. Bearbeitungsstand: 14. November 2016, 11:19 UTC. URL: https://de.wikipedia.org/w/index.php?title=Massenwirkungsgesetz&oldid=159680056 (Abgerufen: 6. Dezember 2016, 13:03 UTC)